Nuevo inhibidor del FGFR3 en modelo de ratón
Una estrategia terapéutica para rescatar el enanismo causado por las mutaciones de incremento de función del FGFR3 es reducir o contrarrestar la hiperactividad de este.
| Muchos tipos de cáncer tienen mutaciones en el FGFR3, en las que el FGFR3 es hiperactivo, lo cual contrasta con su hiperactividad en la acondroplasia, y que reduce el crecimiento. La mutación del FGFR3 en el cáncer aumenta la multiplicación y el crecimiento celular. |
Un grupo de compuestos probados y usados con éxito para reducir el crecimiento del cáncer son los TKIs (inhibidores de la tirosina quinasa), si bien no han sido aplicados hasta ahora en trastornos esqueléticos.
En 2011, un equipo de investigación de Novartis (donde Vito Guagnano era el principal investigador) trabajó en una serie de compuestos existentes (grupo de ureas) y los modificó para crear inhibidores potentes y selectivos de FGFR1, FGFR2 y FGFR3 (receptor de factor de crecimiento de fibroblastos, tirosina quinasas 1, 2, y 3), los TKIs.
En ese momento, uno de los compuestos, llamado NVP-BGJ398 fue seleccionado para su evaluación (pruebas en ratones) in vivo, y mostró un efecto antitumoral significativo en los modelos de xenoinjerto de cáncer de vejiga. Ahí, el equipo de investigación concluyó que los resultados apoyaban el uso terapéutico en potencial del NVP-BGJ38 como un nuevo agente contra el cáncer.
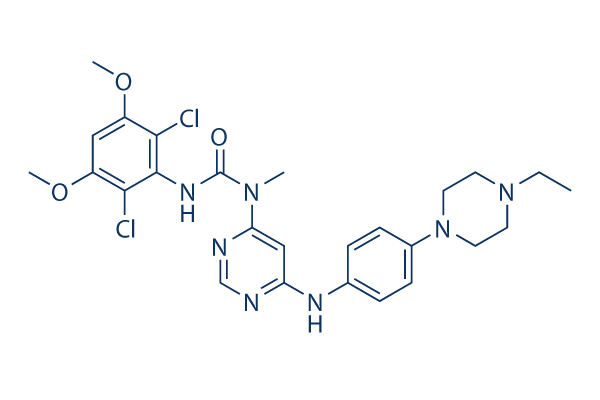
| Estructura química GJ398. Créditos: Selleckchem. |
En enero de 2016, un estudio del Dr. Gudernova, del equipo de investigación liderado por el Prof. Krejci (registro ReACH – República Checa), probó la actividad de 5 inhibidores de la tirosina quinasa (TKIs) contra la señalización en los condrocitos:
- SU5402
- PD173074
- AZD1480
- AZD4547
- BGJ398
Este último compuesto fue el mismo NVP-BGJ398, aunque estos cinco TKIs inhiben fuertemente la activación del FGFR en condrocitos cultivados y alivian completamente la inhibición del FGFR de la proliferación de condrocitos. Sin embargo, cuando fue aplicada en ratones recién nacidos (un organismo vivo y no solamente células en placas de cultivo), los TKIs no mejoraron el crecimiento del esqueleto y tuvieron efectos tóxicos letales en el hígado, los pulmones y los riñones. Así que en un organismo vivo los resultados fueron bastante diferentes y tuvieron efectos secundarios negativos.

| Créditos: Genengnews. |
Si bien las potenciales estrategias terapéuticas para la acondroplasia, que tienen como objetivo reducir la activación excesiva del FGFR3 han surgido con el tiempo, el uso de inhibidores de la tirosina quinasa (TKIs) para contrarrestar la hiperactividad del FGFR3 aún no ha sido evaluado.
DATOS en la Acondroplasia
Recientemente, el 2 de mayo de 2016, el equipo del Prof., Laurence Legeai-Mallet et al. publicó Tyrosine kinase inhibitor NVP-BGJ398 functionally improves FGFR3-related dwarfism in mouse (El inhibidor de la tirosina quinasa NVP-BGJ398 mejora funcionalmente el enanismo relacionado con el FGFR3 en el modelo de ratón)
Aspectos destacados de este documento:
1. El NVP-BGJ398 inhibe la fosforilación del FGFR3 (no permite que el FGFR3 realice sus actividades).
2. El NVP-BGJ398 ha sido identificado como un inhibidor panespecífico de FGFR siendo igualmente activo contra el FGFR1, el FGFR2 y el FGFR3 y menos activo contra el FGFR4 (pan significa "todos").
3. Recientemente, los ensayos de células libres de quinasa mostraron que el NVP-BGJ398 era más selectivo para el FGFR3 que los demás FGFRs.
RESULTADOS
4.En este estudio, el NVP-BGJ398 inhibe la hiperactividad del FGFR3.
5. El NVP-BGJ398 rescató las anomalías de la calota craneana fetal (huesos de la cabeza) y del fémur en cultivos de tejidos de órganos extraídos del modelo de ratón acondroplásico Fgfr3Y367C/+.
|
Ratones Fgfr3Y367C/+: ratones que se desarrollaron en el laboratorio para nacer con displasia tanatofórica, una displasia ósea letal mucho más grave. |
6. La reducción en la actividad del FGFR3 mejoró todas las características patológicas de la acondroplasia en los huesos largos, en la base del cráneo, en el cráneo, en los discos intervertebrales (DIV) y en las vértebras.
|
Regulación hacia abajo de la vía STAT - se restauró la proliferación de condrocitos. Regulación hacia abajo tanto del SOX9 como del MAPK - mejora la diferenciación de los condrocitos. |
7. El alargamiento femoral inducido por NVP-BGJ398 fue dosisdependiente, lo que confirma el papel del FGFR3 como regulador negativo del crecimiento óseo.
8.Los ratones Fgfr3Y367C/+ recién nacidos (P1) fueron tratados diariamente con inyecciones subcutáneas de NVP-BGJ398 (2 mg por kg de peso corporal por día).
9. El NVP-BGJ398 mejora el crecimiento del esqueleto axial (huesos de la cabeza y el tronco) en ratones Fgfr3Y367C/+.
10. Los datos sugieren una posible mejoría con el tratamiento del fenotipo de la estenosis espinal en la acondroplasia.
11. El NVP-BGJ398 mejora el crecimiento del esqueleto craneofacial en ratones Fgfr3Y367C/+.
12. El tratamiento con NVP-BGJ398 previno parcialmente la pérdida de 4 sincondrosis (fusión ósea, sin cartílago).
13. El incremento de crecimiento de los fémures y de las tibias fue un 50% más elevado en animales tratados anteriormente y durante más tiempo con NVP-BGJ398 desde el día 1 que en los tratados desde el día 7.
PRINCIPALES conclusiones
A) El tratamiento con el NVP-BGJ398 también pareció ser más efectivo que el tratamiento con el BMN-111, lo que sugiere que apuntar directamente al FGFR3 con un TKI puede dar un mejor enfoque que apuntar a las vías de señalización descendentes del FGFR3.
B) El tratamiento con el NVP-BGJ398 durante 10 días mejoró el crecimiento óseo 2 a 3 veces más de lo que había sido informado para el BMN111.
14. Los efectos mediados por el NVP-BGJ398 se debieron principalmente a la inhibición del FGFR3, siendo que no se observaron otros efectos secundarios graves.
16. Los efectos relacionados con el tratamiento en el cráneo sugirieron la posibilidad de corregir la apariencia facial en pacientes con acondroplasia y, lo que es más importante, la posibilidad de reducir los riesgos relacionados con la compresión cervicomedular y la muerte temprana que pueden ocurrir en niños con esta condición.
17. Existe la posibilidad de que los tratamientos más prolongados con NVP BGJ398 puedan llevar a un efecto positivo secundario en la estructura ósea resultante.
Protocolos de ESTUDIO
2 protocolos (P) aplicados para tratar ratones FGFR3 Y367C/+
P 1: comienza el día 1 - 15 días de duración
P2: comienza el día 7 - 10 días de duración (parecido al utilizado para el BMN-111)
CONCLUSIÓN
Contamos con dos estudios recientes sobre el NVP-BGJ398, uno que menciona la toxicidad de este compuesto en experimentos in vivo y el otro con datos relevantes que muestran que esta podría ser una posible terapia para la acondroplasia. Es necesaria mucha más investigación sobre esto.


