Mecanismo de Acción del BMN-111
Si bien los pacientes con acondroplasia aún se encuentran limitados a recibir tratamiento por las complicaciones que surgen de su condición, en vez de la condición en sí, se están desarrollando diferentes y prometedores fármacos huérfanos (cuyo objetivo son las enfermedades raras) para el tratamiento de este trastorno genético [1].
El BMN-111 creado por BioMarin (también conocido como Vosoritida) está abriendo un nuevo camino al contar con el primer tratamiento en potencial para que la acondroplasia pueda acceder a un ensayo clínico, el cual en el mes de enero de 2017 ingresó a la Fase III. Al mismo tiempo, otras compañías como ser Therachon AG, están desarrollando otros medicamentos para combatir de otras formas esta enfermedad.
¿Qué es el BMN-111 y cómo trabaja?
 |
 |
 |
|
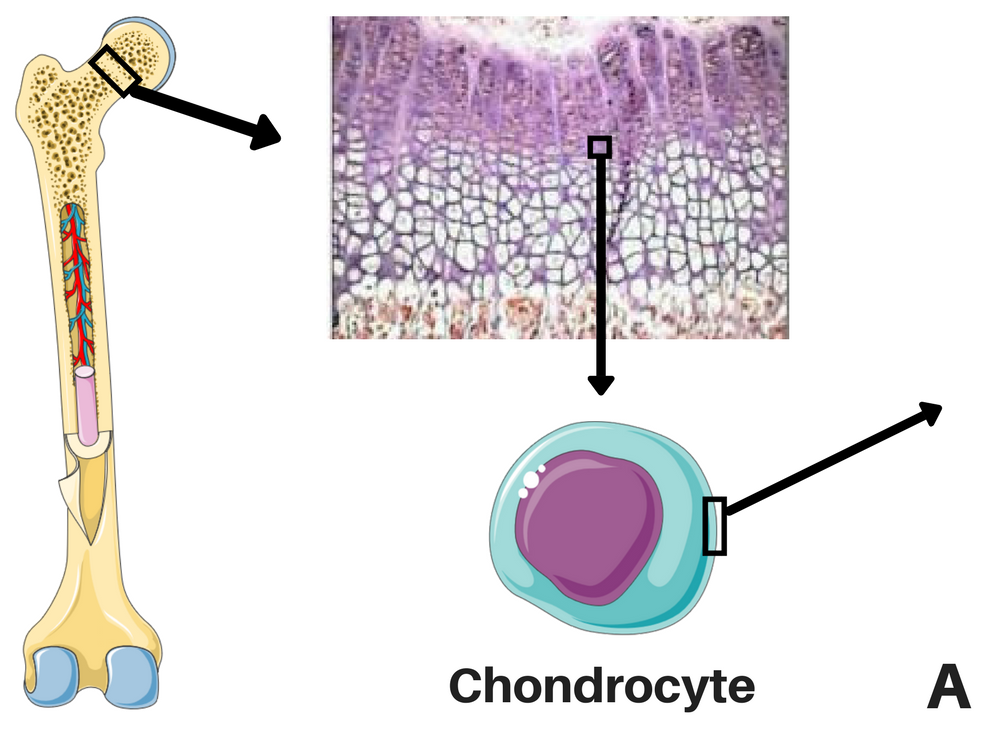
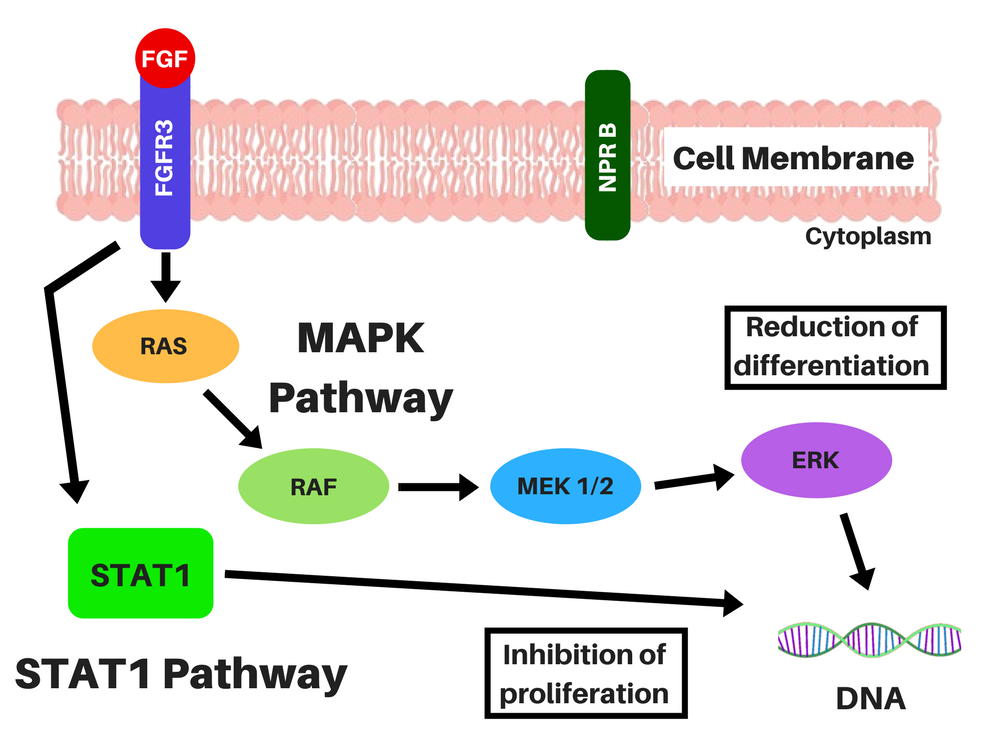
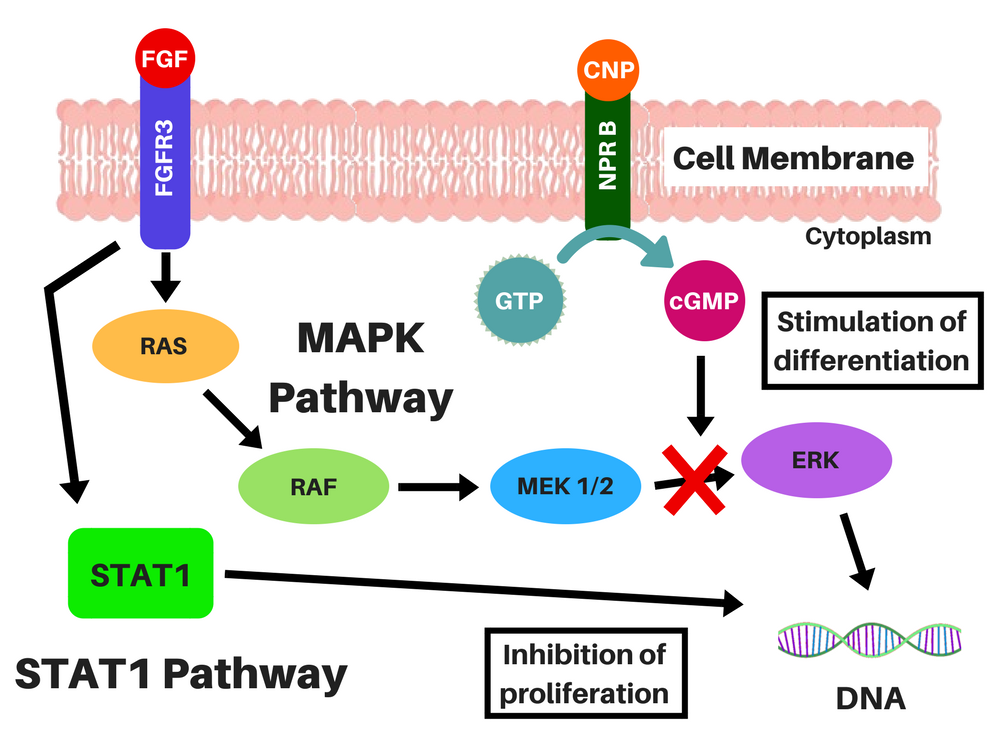
Ubicación de los condrocitos (izquierda) y representaciones de la señalización de FGFR3 sin el CNP (centro), y la acción del CNP y de la vosoritida dentro de una célula (derecha). La vía del STAT-1 disminuye la proliferación y la diferenciación de los condrocitos y la vía del MAPK disminuye la síntesis del ECM por medio de una compleja cascada y reduce la diferenciación de los condrocitos. El CNP induce a la producción de cGMP, el cual inhibirá la acción del MEK1/2 en la vía del MAPK. Créditos: adaptado de Morrys C. Kaisermann. |
Si bien el BMN-111 afecta la vía del MAPK, no llega a afectar la vía STAT-1 (que es la señal que los fármacos, en proceso de desarrollo de la empresa Therachon AG, también tratarán de bloquear). Existe la posibilidad de que las personas afectadas con acondroplasia, con hipoacondroplasia y con displasia tanatofórica puedan ser resistentes al CNP que existe de manera natural [2, 6, 7].
¿Qué efectos ha demostrado tener el BMN-111?
El BMN-111 ha demostrado que reduce el fenotipo acondroplásico, mejorando en el ensayo clínico de Fase II la baja estatura de los pacientes, presentando solamente efectos adversos leves, tales como: reacciones donde se coloca la inyección, dolores de cabeza, hipotensión, dolores de espalda y tos. Sin embargo, todavía no hay datos sobre su eficacia a largo plazo, sobre sus efectos secundarios o sobre cómo afecta en la proporcionalidad del individuo.
¿Qué tan avanzado está su desarrollo?
Este medicamento se encuentra actualmente en ensayo clínico de Fase III. Un estudio de Fase II para niños menores de 5 años está por comenzar en 2018.
Fuentes:
- LEVITEN, M. COMPETING FOR GROWTH. TARGETS & MECHANISMS 2017 [cited 2017 15/06].
- Yasoda, A., et al., Overexpression of CNP in chondrocytes rescues achondroplasia through a MAPK-dependent pathway. Nat Med, 2004. 10(1): p. 80-86.
- Lorget, F., et al., Evaluation of the Therapeutic Potential of a CNP Analog in a <em>Fgfr3</em> Mouse Model Recapitulating Achondroplasia. The American Journal of Human Genetics. 91(6): p. 1108-1114.
- Peake, N.J., et al., Role of C-type natriuretic peptide signalling in maintaining cartilage and bone function. Osteoarthritis and Cartilage, 2014. 22(11): p. 1800-1807.
- Wu, Y., Chen, Y., Qu, R., Lan, T., & Sang, J. (2012). Type II cGMP-dependent protein kinase inhibits EGF-triggered signal transduction of the MAPK/ERK-mediated pathway in gastric cancer cells. Oncology Reports, 27, 553-558.
- Olney, R.C., et al., C-type natriuretic peptide plasma levels are elevated in subjects with achondroplasia, hypochondroplasia, and thanatophoric dysplasia. J Clin Endocrinol Metab, 2015. 100(2): p. E355-9.
- Wendt, D.J., et al., Neutral Endopeptidase-Resistant C-Type Natriuretic Peptide Variant Represents a New Therapeutic Approach for Treatment of Fibroblast Growth Factor Receptor 3–Related Dwarfism. Journal of Pharmacology and Experimental Therapeutics, 2015. 353(1): p. 132.
- BioMarin Presents Vosoritide Data in Achondroplasia at American Society of Human Genetics (ASHG) 2016 Meeting, in GlobeNewswire2016, Nasdaq.


