Механизм действия ТA-46
TA-46 – это новый препарат компании Therachon, предназначенный для применения при ахондроплазии. Данный препарат имеет многообещающие результаты доклинических исследований.
Причиной ахондроплазии является одна точечная мутация в гене, кодирующем рецептор 3 фактора роста фибробластов (FGFR3), которая обусловливает его конститутивную (постоянную) активацию без участия сигнальных молекул, которые обычно требуются для его активации с целью препятствия росту, факторов роста фибробластов (FGF) (более подробно об этом рассказано здесь). Одним из предполагаемых механизмов развития ахондроплазии на молекулярном уровне является то, что в присутствии мутации связывание факторов FGF с FGFR3 дополнительно стабилизирует этот рецептор, затрудняя его разрушение после активации (обычный способ прекращения активности FGFR3 в клетке) [1].
Что такое препарат TA-46, и как он действует?
Вместо воздействия на подавляющую молекулу, как это делает Возоретид - аналог сигнальной молекулы, образующейся в организме в нормальных условиях (натрийуретического пептида типа С), и сигнальной молекулой для подавления одного из сигнальных каскадов FGFR3 (более подробно смотрите здесь) - TA-46 является растворимой формой FGFR3 (sFGFR3), которая захватывает лиганды, факторы FGF, до их связывания с FGFR3 [2], сокращая число связей между FGFs и FGFR3на поверхности клеток и хотя бы отчасти снижая избыточную активность рецептора.
 |
 |
 |
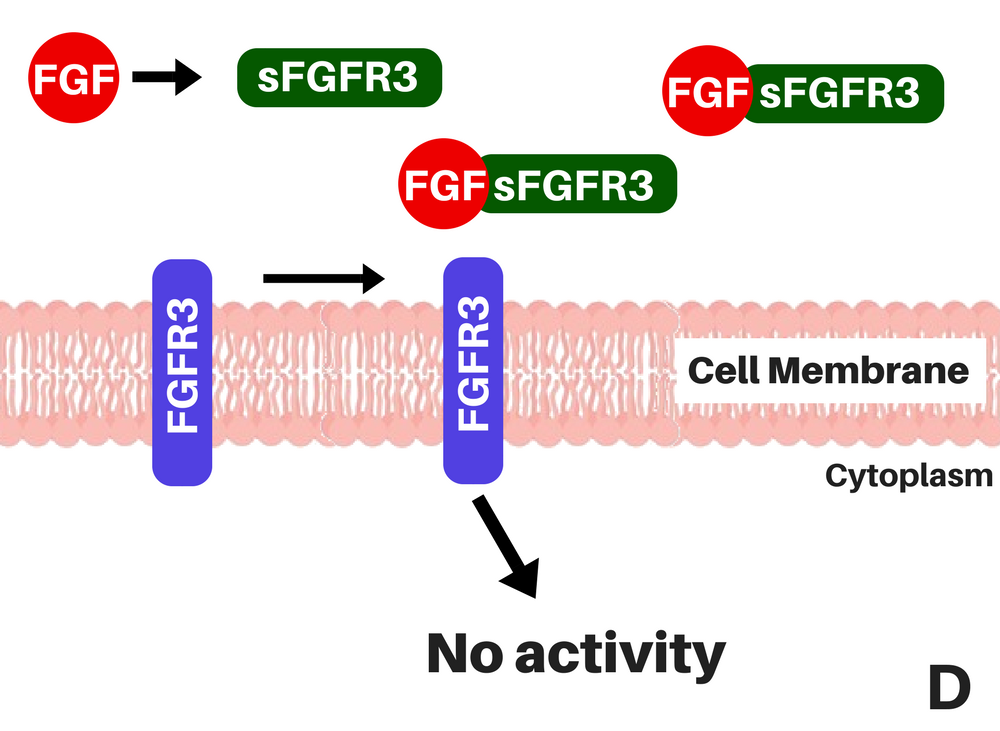 |
| Место расположения хондроцитов в кости (A), обычный механизм действия FGFR3 (B), механизм действия при ахондроплазии (C), и механизм действия sFGFR3 (TA-46) (D). Это происходит на поверхности хондроцитов, в пластинке роста трубчатых костей (т.е., в костях бедра). По материалам: Therachon. |
На какой стадии разработки находится препарат TA-46?
Результаты доклинических исследований на мышах свидетельствуют о способности TA-46 восстанавливать рост костей и устранять нарушения обмена веществ в костной ткани, с которыми связано развитие ахондроплазии. sFGFR3 отнесен к категории Лекарственных средств, предназначенных для лечения редких заболеваний у детей. Данная категория была присвоена ему как FDA (Управлением по контролю качества пищевых продуктов и лекарственных препаратов США), так и EMA (Европейским агентством по оценке лекарственных средств). Начало клинических испытаний 1 фазы планируется на начало 2018 г. [3].
Источники
- Cho, J.Y., et al., Defective lysosomal targeting of activated fibroblast growth factor receptor 3 in achondroplasia. Proc Natl Acad Sci U S A, 2004. 101(2): p. 609-14.
- Therachon. Research. 2017 [cited 2017 25/05].
- Therachon Announces Dosing of First Subject in Phase 1 Clinical Trial Evaluating TA-46, a Novel Investigational Therapy for the Potential Treatment of Achondroplasia, Business Wire [cited 23/06].
- Therachon Announces Start of Natural History Study in Children with Achondroplasia, Business Wire [cited 23/06].


